首例新冠危重症患者全肺活检病理报告:提示肺部病变起源部位
新冠肺炎病理目前仍有待深入研究。除华中科技大学刘良等人实施的遗体解剖之外,部分科研团队也在从组织活检渠道获取病理分析。中科院院士、国家感染性疾病临床医学研究中心主任王福生教授率领的团队,武汉大学中南医院肖书渊主任医师团队此前也均发布相关病理发现。
当地时间3月2日,深圳市第三人民医院(南方科技大学第二附属医院)、国家感染性疾病临床医学研究中心的研究团队在预印本网站Preprints更新发布了“新型冠状病毒肺炎危重症患者的临床病理分析”(Clinical pathology of critical patient with novel coronavirus pneumonia (COVID-19),最早于2月27日发布第一版),该研究尚未经同行评议。
研究团队对1例进行了肺移植手术的危重症新冠肺炎患者的全肺进行了活检,通过HE染色、免疫组织化学染色和特殊染色(包括Masson染色、PAS染色和六胺银染色)对其病理变化进行了描述。全肺组织呈弥漫性充血或部分出血坏死。右肺右叶外缘明显可见出血性坏死。肺切面有严重的充血和出血改变。
研究团队称,他们首次描述了新冠肺炎危重症患者的主要病理变化。该研究展示了危重症患者的临床病理活检,这可能为深入了解该病的发病机制和严重程度提供了依据。
该论文通讯作者之一为深圳市第三人民医院院长兼党委书记、主任医师刘磊教授。据医院官网介绍,国家感染性疾病临床医学研究中心、深圳市第三人民医院是深圳唯一收治新冠肺炎确诊患者的定点医院,也是除湖北省外,单中心收治新冠肺炎患者最多的医院。此外,医院拥有占地面积391平方米的P3实验室,具有开展新冠病毒肺炎系列研究的临床资源和研究综合条件。
截至目前,关于流行病学和临床特征的研究已不断累积。多数患者出现发热、咳嗽等症状,但小部分患者出现急性呼吸衰竭、急性呼吸窘迫综合征(ARDS)、感染性休克等严重并发症。值得注意的是,目前来看,新冠肺炎的危重症患者预后差,死亡率高。
研究中这例患者66岁,2020年1月4日从武汉返回深圳,并出现高热和咳嗽症状。除8年高血压病史外,无其他基础疾病,心功能良好。胸部X线检查可见左右肺亮度增高、多发阴影。该例患者被诊断为新冠肺炎(危重型)和严重ARDS,并发呼吸衰竭,行肺移植手术。
研究团队在P3实验室对肺病理组织进行了固定、脱水、石蜡包埋、组织切片、特殊组织化学染色等。
结果显示,该病例全肺表面呈古铜色,肉眼可见弥漫性充血,多为点状出血,部分出血坏死。值得注意的是,出血坏死主要发生在肺右下叶、中叶和上叶的外边缘。支气管被粘液和出血渗出物覆盖。肺切面有严重的充血和出血改变。
组织病理学表现为大量的肺间质纤维化伴部分透明变性,肺出血性梗死。小血管增生,血管壁增厚,管腔狭窄闭塞。炎症细胞间质浸润,包括淋巴细胞、浆细胞和单核细胞。经Masson染色证实肺间质纤维化。未见其他细菌、真菌感染。
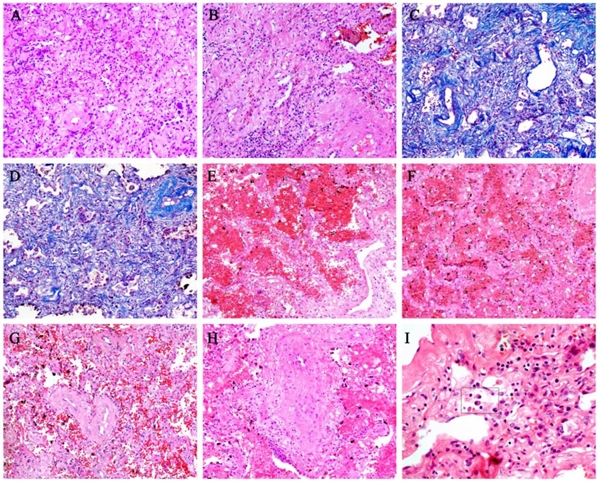
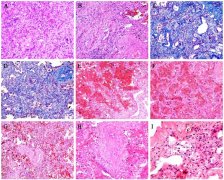
危重病人肺间质组织病理活检:A、大量肺间质纤维化。B、肺间质纤维化伴部分透明变性。C、Masson染色肺间质纤维化。D、Masson染色间质纤维化,肺泡上皮细胞脱屑。E、肺出血改变。F、肺出血性梗死。G、血管壁增厚,管腔狭窄。H、闭塞性脉管炎由炎性细胞包围。I、间质浆细胞浸润(方框示意)。
可见肺泡炎伴肺泡上皮细胞(主要为II型)的萎缩、增殖、脱屑及鳞状上皮化生的各种改变。其余肺泡显示肺泡隔增厚,肺泡上皮细胞坏死、脱屑。此外,还观察到大量纤维素样渗出物、多核巨细胞和胞浆内病毒包涵体。坏死性细支气管炎表现为细支气管壁坏死,管腔内可见上皮细胞。
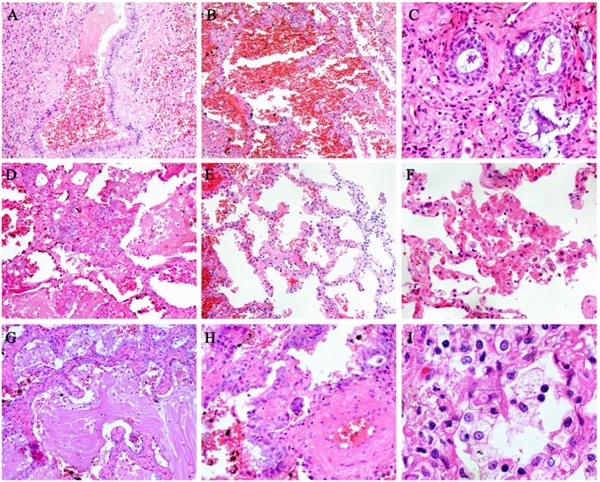
COVID-19肺泡改变活检。A、坏死性细支气管炎,腔内可见坏死的支气管上皮细胞。B、肺泡上皮细胞萎缩。C、细支气管上皮细胞鳞状上皮化生。D、肺泡细胞鳞状上皮化生。E、肺泡隔增厚。F、肺泡上皮细胞坏死、脱屑。G、腔内有炎性细胞和大量纤维素样渗出物。H、多核巨细胞。I、肺泡上皮细胞胞浆内病毒包涵体(方框示意)。
免疫组织学结果显示,CD3、CD4、CD8、CD20、CD79a、CD5和CD38等免疫细胞呈阳性。研究发现免疫细胞的阳性表达主要集中在肺间质和血管附近。此外,CD31、TTF1、CK5/6、CK7、CK19、SMA、F VIII和IV型胶原也呈阳性(部分数据未显示)。
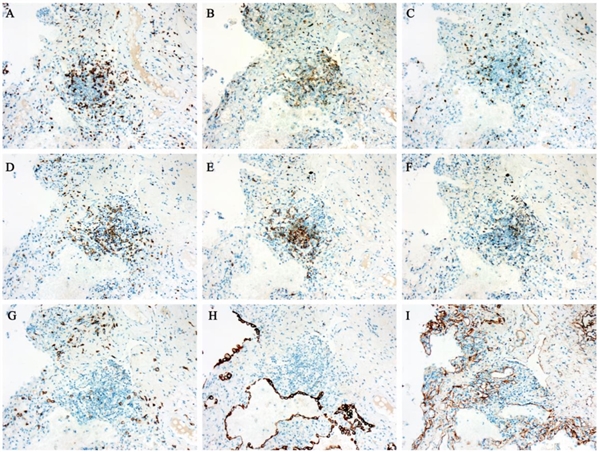
危重症COVID-19免疫组织学结果。连续组织切片显示CD3 (A)、CD4 (B)、CD8 (C)、CD20 (D)、CD79a (E)、CD5 (F)、CD38 (G)、CK7 (H)、IV型胶原(I)阳性表达。